2016年美国国会通过了《21世纪治愈法案》,明确了FDA可以在合适情况下使用真实世界数据(RWD),作为医疗器械及药品上市后研究及新适应症开发的审批证据。2019年5月29日国家药品审评中心发布中国《真实世界证据支持药物研发的基本考虑(征求意见稿)》;2020年1月7日,NMPA发布了《真实世界证据支持药物研发与审评的指导原则(试行)》,为制药企业的药物研发给出明确的信号和政策保障。2020年3月我国首个使用境内真实世界数据的医疗器械产品获批上市。
国内外政策的大力支持,让真实世界研究成为行业关注焦点。众多企业都将真实世界研究(RWS)作为新适应症拓展、精准用药模型和精准治疗模型构建的重要方式。在国家“4+7”政策和两票制政策的压力之下,多家药企巨头更是将RWS作为药品上市后学术推广的新方向,变革传统的药品医学知识传递和应用方式,已在医院和leading PI等相关领域积极布局,筹划多种合作形式。
另一方面,真实世界研究(RWS)尚存在众多亟需解决的问题。真实世界数据(RWD)不等于证据(RWE)。RWD的收集面临着数据的质量、数据编码的差异问题、院外的数据收集等众多挑战;同时研究样本量大、数据异质性强,对统计方法的要求比就更高,多属于回顾性分析或事后分析,研究证据等级受到挑战。
我国真实世界研究尚处于起步阶段,使用信息化+AI技术助力企业开展RWS研究,可以实现弯道超车。百奥知依靠13年对临床研究的深刻理解,应用AI和大数据技术开创了基于智能分析模型实施的目标导向型RWS解决方案。
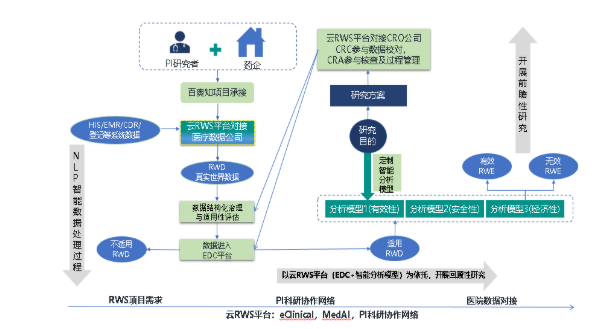
利用信息化与AI技术一方面可以打通横亘在临床数据收集过程中的多种系统(如HIS、EMR)障碍,将存在于真实世界中的患者和药品数据实现精准提取,形成病人画像和研究知识库,在基于云服务的真实世界研究一体化云平台下,可以帮助临床研究者实现患者智能招募、基于风险的远程监查,大幅降低真实世界研究的数据采集和项目运营成本,提升真实世界研究的成果产出效率。另一方面,可以帮助研究发起方充分掌握研究背景 ,提出有创新性的研究设想和完善的研究设计,提供可利用的多源数据和强大的统计分析,保证了数据的多元性、重要性和时效性。
基于智能分析模型实施的目标导向型RWS解决方案,把智能化的数据处理,及信息化的数据收集,跟智能分析模型相结合实现整理和收集数据的同时,随时进行数据分析,随时查看分析结果。相比传统的研究实施过程可以在很大程度上降低研究的成本。很简单的一个例子,假如通常一个研究需要收集的病例数为1000,在收集到500的时候,分析结果已经达到最初研究目的需求时,就可以考虑调整实施策略;而且,对数据随时进行分析,还可能发现一些意外分析结果,帮助研究者调整研究方案,获取更大的研究成果。对企业来说,就可以在同样的成本下,获取更高的研究获益。
对于真实世界研究RWS而言,无论是政策环境还是研究层面,都迎来了良好的发展时机。信息化和AI大数据技术在真实世界研究的价值必将始于数据收集,着力于数据汇集,实现于数据医学价值挖掘和商业价值延伸!百奥知立足于信息化和AI大数据技术,与行业合作伙伴携手同行,助力我国真实世界研究的高效运行!