
2020年1月7日,NMPA发布了首个真实世界研究RWS相关指导原则:《真实世界证据支持药物研发与审评的指导原则(试行)》,为制药企业的药物RWS研究给出明确的信号和政策保障。随后,2020年8月27日,国家药监局药审中心发布《真实世界研究支持儿童药物研发与审评的技术指导原则(试行)》(2020年第22号),为儿童药物RWS研究提供指导。随着大数据时代到来,在国内外政策的大力支持下,药物RWS方兴未艾,未来可期。
1、 数据来源广泛
真实世界数据(RWD),数据类型从研究数据到非研究数据,存在多种产生渠道,如何快速得到可靠的真实世界数据是决定RWS研究成败的重要要素。
2、 证据质量难保障
真实世界数据(RWD)不等于证据(RWE)RWD的收集面临着数据的质量、数据编码的差异问题、院外的数据收集等众多挑战;同时研究样本量大、数据异质性强,对统计方法的要求比就更高,多属于回顾性分析或事后分析,研究证据等级受到挑战。
3、 应用与实施经验尚浅
尤其在真实世界研究的设计原则、实施方法、数据分析等方面认知尚浅。
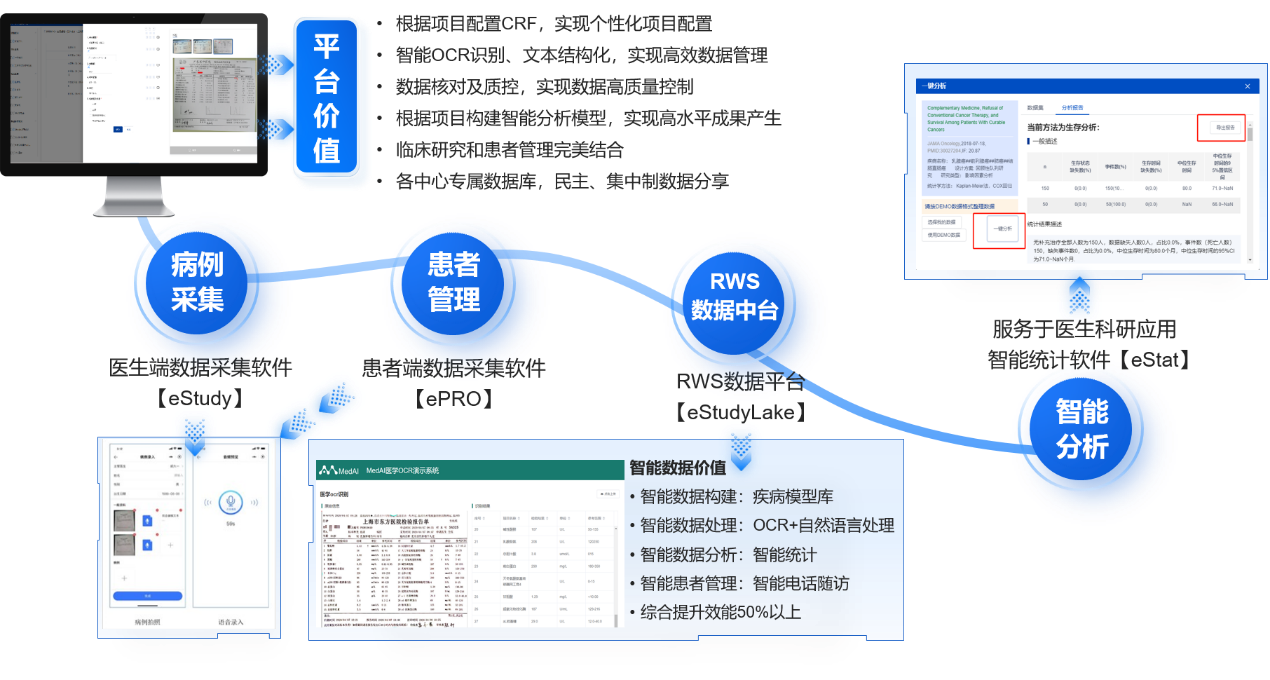
百奥知易科研-云RWS解决方案为真实世界研究插上信息化+AI的翅膀
百奥知依靠十多年对临床研究的深刻理解,应用AI和大数据技术开创了基于智能分析模型实施的目标导向型RWS解决方案——易科研平台。
利用信息化与AI技术打通横亘在临床数据收集过程中的多种系统(如HIS、EMR)障碍,精准提取患者与药品数据,在基于云服务的真实世界研究一体化云平台下,帮助临床研究者实现患者招募、远程监查等大幅降低数据采集和项目运营成本,提升RWS的成果产出效率。同时,还可以帮助研究发起方充分掌握研究背景 ,提出有创新性的研究设想和完善的研究设计,提供可利用的多源数据和强大的统计分析,保证了数据的多元性、重要性和时效性。