
药物警戒工作贯穿药品的整个生命周期,是保障质量和安全的防线,也是管理与控制风险的重要活动。在新版GCP与GVP等政策要求下,药物警戒工作的要求难度大幅提升,传统工作模式难以满足日益严格的监管要求,因此通过数字化技术,线上化进行药物警戒工作已经成为趋势。
Bioknow PV 系统深耕行业 6 年+,致力于打造中国式独一无二的药物警戒解决方案。作为国内最早的一批药物警戒系统,Bioknow PV 汇集国内外主流产品的优点,并结合行业专家、客户反馈,以及对行业、法规的理解,经过数百次产品迭代,目前已获得300多家客户的深度认可。
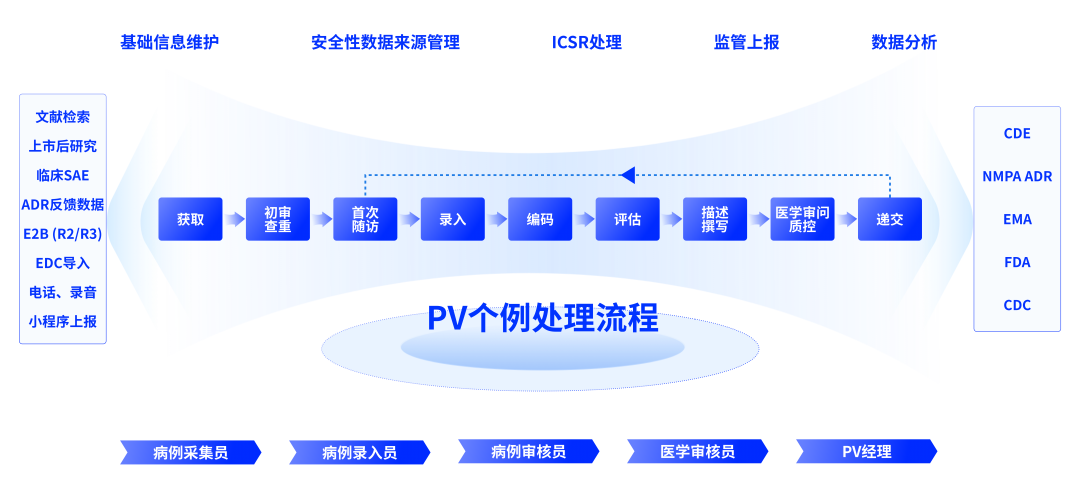
Bioknow PV 系统是个例报告、定期报告、随访管理等一系列警戒安全事宜的一站式管家。支持多渠道主动采集与自动采集、审查、录入、审核、研究、评估、评价、病例自动撰写、数据分析、主动与自动递交。并支持建立药物警戒管理体系,助力企业合规、高效、高质、及时、可持续性管理药物安全性数据与资料。
个例处理流程
产品优势
Bioknow PV系统已完成E2B Gateway对接国家药品监督管理局药品评价中心(NMPA CDR)、国家药品监督管理局药品审评中心(NMPA CDE)、美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)等药监部门,并已成功为客户实施部署了中美双报英文药物警戒系统。
① 支持小程序与PC双端无缝同步。
② 支持个例报告填写表单、报告列表展示、 工作流程、搜索字段、去重字段等的自定义配置。
③不限制账户数量,满足客户的多样化需求。
提供多样性的提醒功能,在第一时间获取不良事件后,通过邮件等渠道快速通知相关人员,结合信号检测,使不良事件更容易监控与处理。
满足法规对于不良事件需要24小时内上报药物警戒部门,SUSAR需要7-15天递交监管机构的要求。
① 定期回访
定期回访及时了解软件使用情况,提供电话咨询和远程支持服务。
② 培训服务
为客户的系统管理员或系统操作者提供软件使用方面的专业培训服务,支持在线培训与现场培训。
③ 电话支持
法定工作时间享受不限次数的电话支持;紧急情况下可及时联系到相关对接人员。
系统支持云端部署与本地部署,全面覆盖各种应用场景。每种部署方式均包含日常使用的生产环境、验证与培训使用的测试环境、灾备使用的灾备环境,以及全面的稽查机制,让客户用的更放心。
核心功能